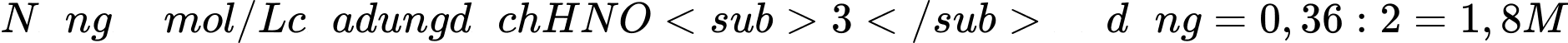Chia hỗn hợp gồm Mg và MgO thành hai phần bằng nhau:
- Phần 1: Cho tác dụng hết với dung dịch HCl thu được 3,4706 lít H2 (đkc), dung dịch sau phản ứng chứa 14,25 gam muối.
- Phần 2: Hòa tan hoàn toàn bằng lượng vừa đủ 200 mL dung dịch HNO3 thì thu được 0,02 mol khí X.
a) Tìm công thức phân tử của khí X.
b) Tính nồng độ mol/L của dung dịch HNO3 đã dùng.
-
-
-
-
Đáp án đúng:
a) Phần 1: Số mol H2 = 0,14 mol
Mg + 2HCl  MgCl2 + H2
MgCl2 + H2
MgO + 2HCl  MgCl2 + H2O
MgCl2 + H2O
Số mol Mg = Số mol H2 = 0,14 mol
Số mol MgCl2 = Số mol Mg + Số mol MgO
 0,15 = 0,14 + nMgO
0,15 = 0,14 + nMgO  nMgO = 0,01 mol
nMgO = 0,01 mol
Phần 2: Số mol Mg(NO3)2 = Số mol Mg + Số mol MgO = 0,15 mol
Khối lượng Mg(NO3)2 = 149.0,15 = 22,2 gam < 23 gam  Có muối NH4NO3 tạo thành.
Có muối NH4NO3 tạo thành.
Số mol NH4NO3 = (23 – 22,2)/80 = 0,01 mol
Các quá trình oxi hóa - khử
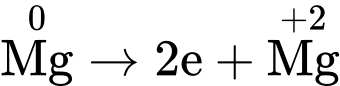
0,14 mol 0,28 mol

0,08 mol 0,01 mol
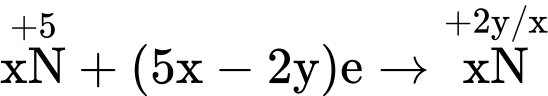
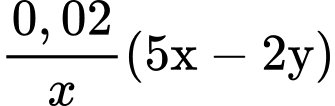 mol 0,02 mol
mol 0,02 mol
Áp dụng bảo toàn electron: 0,28 = 0,08 + (5x – 2y)0,02/x  10x = 5x – 2y.
10x = 5x – 2y.
 Nghiệm hợp lí x = 2, y = 0. Chất khí X là N2.
Nghiệm hợp lí x = 2, y = 0. Chất khí X là N2.
b) Số mol HNO3 phản ứng =  = 0,15.2 + 0,01.2 + 0,02.2 = 0,36 mol
= 0,15.2 + 0,01.2 + 0,02.2 = 0,36 mol
\Rightarrow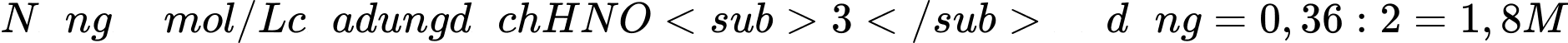 Số bình luận về đáp án: 1
Số bình luận về đáp án: 1
Mg + 2HCl
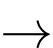 MgCl2 + H2
MgCl2 + H2
MgO + 2HCl
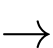 MgCl2 + H2O
MgCl2 + H2O
Số mol Mg = Số mol H2 = 0,14 mol
Số mol MgCl2 = Số mol Mg + Số mol MgO
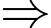 0,15 = 0,14 + nMgO
0,15 = 0,14 + nMgO 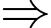 nMgO = 0,01 mol
nMgO = 0,01 mol
Phần 2: Số mol Mg(NO3)2 = Số mol Mg + Số mol MgO = 0,15 mol
Khối lượng Mg(NO3)2 = 149.0,15 = 22,2 gam < 23 gam
 Có muối NH4NO3 tạo thành.
Có muối NH4NO3 tạo thành.
Số mol NH4NO3 = (23 – 22,2)/80 = 0,01 mol
Các quá trình oxi hóa - khử
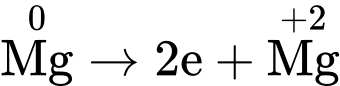
0,14 mol 0,28 mol

0,08 mol 0,01 mol
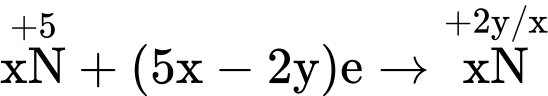
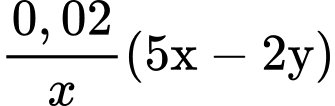 mol 0,02 mol
mol 0,02 mol
Áp dụng bảo toàn electron: 0,28 = 0,08 + (5x – 2y)0,02/x
 10x = 5x – 2y.
10x = 5x – 2y.
 Nghiệm hợp lí x = 2, y = 0. Chất khí X là N2.
Nghiệm hợp lí x = 2, y = 0. Chất khí X là N2.
b) Số mol HNO3 phản ứng =
 = 0,15.2 + 0,01.2 + 0,02.2 = 0,36 mol
= 0,15.2 + 0,01.2 + 0,02.2 = 0,36 mol
\Rightarrow