Cho 12,25 gam KClO3 vào dung dịch HCl đặc dư, khí Cl2 thoát ra cho tác dụng hết với kim loại M thu được 38,10 gam hỗn hợp chất rắn X. Cho X vào dung dịch AgNO3 dư, thu được 118,5 gam kết tủa. Các phản ứng đều xảy ra hoàn toàn. Kim loại M là
-
-
-
-
Đáp án đúng: C
Giải: Ta có nKClO3 = 0,1 mol || Pứ KClO3 + 6HCl → KCl + 3Cl2 + 3H2O
⇒ mCl2 = 0,3×71 = 21,3 gam || Bảo toàn nguyên tố Cl → nAgCl = 0,6 mol
 mAgCl = 86,1 gam < 118,5 gam ⇒ mAg = 32,4 gam ⇒ nAg = 0,3 mol
mAgCl = 86,1 gam < 118,5 gam ⇒ mAg = 32,4 gam ⇒ nAg = 0,3 mol
+ Bảo toàn khối lượng ta có mM = 38,1 – 21,3 = 16,8 gam
+ Gọi kim loại M có hóa trị n ||⇒ Bảo toàn e ta có:
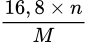 = 2nCl2 + nAg
= 2nCl2 + nAg  M =
M = 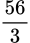 × n
× n
⇒ M = 56 ứng với n = 3 ⇒ Chọn C
Số bình luận về đáp án: 5
⇒ mCl2 = 0,3×71 = 21,3 gam || Bảo toàn nguyên tố Cl → nAgCl = 0,6 mol
 mAgCl = 86,1 gam < 118,5 gam ⇒ mAg = 32,4 gam ⇒ nAg = 0,3 mol
mAgCl = 86,1 gam < 118,5 gam ⇒ mAg = 32,4 gam ⇒ nAg = 0,3 mol+ Bảo toàn khối lượng ta có mM = 38,1 – 21,3 = 16,8 gam
+ Gọi kim loại M có hóa trị n ||⇒ Bảo toàn e ta có:
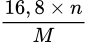 = 2nCl2 + nAg
= 2nCl2 + nAg  M =
M = 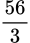 × n
× n⇒ M = 56 ứng với n = 3 ⇒ Chọn C