Cho 200 ml dung dịch X chứa hỗn hợp H2SO4 aM và HCl 0,1M tác dụng với 300 ml dung dịch Y chứa hỗn hợp Ba(OH)2 bM và KOH 0,05M thu được 2,33 gam kết tủa và dung dịch Z có pH = 12. Giá trị của a và b lần lượt là
-
-
-
-
Đáp án đúng: D
Có nH+ = 0,4a + 0,02 mol, nOH- = 0,6b + 0,015 mol, nBa2+ = 0,3b, nSO42-= 0,2a , nBaSO4 = 0,01 mol
Phương trình pư :H+ + OH- → H2O, SO42- + Ba2+ → BaSO4 ↓
Vì dung dịch Z có pH = 12 nên dung dịch Z còn OH- → nOH-dư = 0,01. 0,5 = 0,005 mol
Ta có nOH- dư = nOH- - nH+ = 0,6b + 0,015 - 0,4a- 0,02= 0,6b - 0,4a -0,005 = 0,005 (1)
Nếu nSO42- > nBa2+ → nBaSO4 = nBa2+ = 0,01 → 0,3b = 0,01 → b= 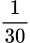 . Thay vào (1)→ a= 0,025 (Không thỏa mãn điều kiện nSO42- > nBa2+ )
. Thay vào (1)→ a= 0,025 (Không thỏa mãn điều kiện nSO42- > nBa2+ )
Nếu nSO42- < nBa2+ → nBaSO4 = nSO42- = 0,01 → 0,2a = 0,01 → a= 0,05. Thay vào (1) → b = 0,05 . Vậy đáp án D.
Số bình luận về đáp án: 1
Phương trình pư :H+ + OH- → H2O, SO42- + Ba2+ → BaSO4 ↓
Vì dung dịch Z có pH = 12 nên dung dịch Z còn OH- → nOH-dư = 0,01. 0,5 = 0,005 mol
Ta có nOH- dư = nOH- - nH+ = 0,6b + 0,015 - 0,4a- 0,02= 0,6b - 0,4a -0,005 = 0,005 (1)
Nếu nSO42- > nBa2+ → nBaSO4 = nBa2+ = 0,01 → 0,3b = 0,01 → b=
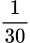 . Thay vào (1)→ a= 0,025 (Không thỏa mãn điều kiện nSO42- > nBa2+ )
. Thay vào (1)→ a= 0,025 (Không thỏa mãn điều kiện nSO42- > nBa2+ )Nếu nSO42- < nBa2+ → nBaSO4 = nSO42- = 0,01 → 0,2a = 0,01 → a= 0,05. Thay vào (1) → b = 0,05 . Vậy đáp án D.