Cho cân bằng hóa học sau: 2SO2 (k) + O2 (k) 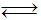 2SO3 (k) ; ΔH < 0
2SO3 (k) ; ΔH < 0
Cho các biện pháp : (1) tăng nhiệt độ, (2) tăng áp suất chung của hệ phản ứng, (3) hạ nhiệt độ, (4) dùng thêm chất xúc tác V2O5, (5) giảm nồng độ SO3, (6) giảm áp suất chung của hệ phản ứng. Những biện pháp nào làm cân bằng trên chuyển dịch theo chiều thuận?
-
-
-
-
Đáp án đúng: D
HD:
Xét các yếu tố:
(1). Tăng nhiệt độ → cân bằng chuyển dịch về phía làm giảm nhiệt độ (theo chiều thu nhiệt ∆H <0)
→ cân bằng chuyển dịch theo chiều nghịch.
(2). Áp suất tỷ lệ với số mol → áp suất trước phản ứng > áp suất sau phản ứng. Khi tăng áp suất
chung của hệ → cân bằng chuyển dịch về phía làm giảm áp suất → cân bằng chuyển dịch theo chiều thuận.
(3). Hạ nhiệt độ → cân bằng chuyển dịch về phía làm tăng nhiệt độ (theo chiều tỏa nhiệt ∆ H <0)
→ cân bằng chuyển dịch theo chiều thuận.
(4). Chất xúc tác V2O5 không làm chuyển dịch cân bằng mà chỉ làm tăng tốc độ phản ứng thuận và nghịch.
(5). Giảm nồng độ SO3 → cân bằng chuyển dịch về phía làm tăng nồng độ SO3
→ cân bằng chuyển dịch theo chiều thuận.
(6). Cân bằng chuyển dịch theo chiều nghịch.
Chọn D.
Số bình luận về đáp án: 0
Xét các yếu tố:
(1). Tăng nhiệt độ → cân bằng chuyển dịch về phía làm giảm nhiệt độ (theo chiều thu nhiệt ∆H <0)
→ cân bằng chuyển dịch theo chiều nghịch.
(2). Áp suất tỷ lệ với số mol → áp suất trước phản ứng > áp suất sau phản ứng. Khi tăng áp suất
chung của hệ → cân bằng chuyển dịch về phía làm giảm áp suất → cân bằng chuyển dịch theo chiều thuận.
(3). Hạ nhiệt độ → cân bằng chuyển dịch về phía làm tăng nhiệt độ (theo chiều tỏa nhiệt ∆ H <0)
→ cân bằng chuyển dịch theo chiều thuận.
(4). Chất xúc tác V2O5 không làm chuyển dịch cân bằng mà chỉ làm tăng tốc độ phản ứng thuận và nghịch.
(5). Giảm nồng độ SO3 → cân bằng chuyển dịch về phía làm tăng nồng độ SO3
→ cân bằng chuyển dịch theo chiều thuận.
(6). Cân bằng chuyển dịch theo chiều nghịch.
Chọn D.