Cho dung dịch FeCl2 nồng độ 10% phản ứng vừa đủ với dung dịch NaOH nồng độ 20%. Đun nóng trong không khí để phản ứng xảy ra hoàn toàn. Tính nồng độ phần trăm của muối trong dung dịch sau phản ứng (coi nước bay hơi không đáng kể).
-
-
-
-
Đáp án đúng: D
HD: để tính nhanh hơn, ta cho: nFeCl2 = 1 mol → mdd FeCl2 = 1270 gam.
NaOH phản ứng vừa đủ nên theo tỉ lệ có: n NaOH = 2 mol → mdd NaOH = 40 gam.
Khi đun nóng trong không khí để phản ứng hoàn toàn ta chú ý:
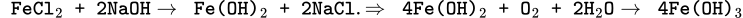
Như vậy, sau phản ứng, tổng khối lượng dung dịch là:
m = mdd FeCl2 + m dd NaOH + mO2 - mFe(OH)3 = 1270 + 400 + 8 - 107 = 1571 gam.
Và muối duy nhất trong dung dịch là 2 mol NaCl. Vậy nồng độ phần trăm của muối là:
C = 2 × 58,5 ÷ 1571 = 7,45 %.
Chú ý oxi của không khí để tránh nhầm với đáp án C. Đáp án đúng là D.♠♠♠
Số bình luận về đáp án: 24
NaOH phản ứng vừa đủ nên theo tỉ lệ có: n NaOH = 2 mol → mdd NaOH = 40 gam.
Khi đun nóng trong không khí để phản ứng hoàn toàn ta chú ý:
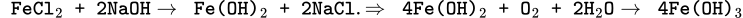
Như vậy, sau phản ứng, tổng khối lượng dung dịch là:
m = mdd FeCl2 + m dd NaOH + mO2 - mFe(OH)3 = 1270 + 400 + 8 - 107 = 1571 gam.
Và muối duy nhất trong dung dịch là 2 mol NaCl. Vậy nồng độ phần trăm của muối là:
C = 2 × 58,5 ÷ 1571 = 7,45 %.
Chú ý oxi của không khí để tránh nhầm với đáp án C. Đáp án đúng là D.♠♠♠