Cho một lượng CuSO4.5H2O vào 100 ml dung dịch AgNO3 1M thu được dung dịch X. Tiến hành điện phân dung dịch X bằng điện c?
Cho một lượng CuSO4.5H2O vào 100 ml dung dịch AgNO3 1M thu được dung dịch X. Tiến hành điện phân dung dịch X bằng điện cực trơ tới khi khối lượng catot tăng m gam thì dừng điện phân. Dung dịch sau điện phân hòa tan tối đa 14,0 gam bột Fe thu được dung dịch Y (không chứa ion 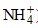 ) và hỗn hợp khí Z gồm 2 khí không màu trong đó có một khí hóa nâu trong không khí. Tỉ khối hơi của Z so với H2 bằng
) và hỗn hợp khí Z gồm 2 khí không màu trong đó có một khí hóa nâu trong không khí. Tỉ khối hơi của Z so với H2 bằng 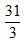 . Giá trị m là
. Giá trị m là
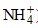 ) và hỗn hợp khí Z gồm 2 khí không màu trong đó có một khí hóa nâu trong không khí. Tỉ khối hơi của Z so với H2 bằng
) và hỗn hợp khí Z gồm 2 khí không màu trong đó có một khí hóa nâu trong không khí. Tỉ khối hơi của Z so với H2 bằng 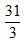 . Giá trị m là
. Giá trị m là
A. 26,8.
B. 30,0.
C. 23,6.
D. 20,4.
Đáp án C
Giải: Ta có MZ = \(\dfrac{62}{3}\) ⇒ Z chứa H2 || 1 khí hóa nâu trong không khí ⇒ Z gồm NO và H2Dùng sơ đồ đường chéo ⇒ nNO: nH2 = 2:1 || Do sinh khí H2 ⇒ NO3– bị khử hết
Bảo toàn nguyên tố Nitơ: nNO = nNO3– = 0,1 mol ⇒ nH2 = 0,05 mol
4H+ + NO3– + 3e → NO + 2H2O || 2H+ + 2e → H2 ⇒ nH+ = 0,5 mol
Bảo toàn electron: 2nCu2+ + nAg+ = nH+ ⇒ nCu2+ pứ = 0,2 mol
||⇒ m = 0,2× 64 + 0,1× 108 = 23,6 gam ⇒ Chọn C







