Cho phương trình phản ứng: Mg + HNO3 → Mg(NO3)2 + NO + N2O + H2O.
Nếu tỉ khối của hỗn hợp NO và N2O đối với H2 là 19,2. Tỉ lệ số phân tử bị khử và bị oxi hóa là
-
-
-
-
Đáp án đúng: A
Giải: MNO, N2O = 19,2 × 2 = 38,4 ⇒ 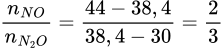 .
.
► Quá trình cho-nhận e: Mg → Mg+2 + 2e (1) || 8N+5 + 30e → 2N+2 + 6N+1 (2).
Thăng bằng electron: 15 × (1) + 1 × (2) ⇒ 15Mg + 8N+5 → 15Mg+2 + 2N+2 + 6N+1.
● Điền hệ số: 15Mg + HNO3 → 15Mg(NO3)2 + 2NO + 3N2O + H2O.
Chú ý: chưa điền hệ số vào HNO3 vì 1 phần N+5 (NO3–) đóng vai trò môi trường.
Bảo toàn nguyên tố Nitơ ⇒ 38HNO3. Bảo toàn nguyên tố Hidro ⇒ 19H2O.
||⇒ 15Mg + 38HNO3 → 15Mg(NO3)2 + 2NO + 3N2O + 19H2O.
► Phân tử bị khử là N trong sản phẩm khử (cụ thể là NO và N2O),
phân tử bị oxi hóa là Mg ⇒ tỉ lệ là (2 + 3 × 2) : 15 = 8 : 15 ⇒ chọn A.
Số bình luận về đáp án: 14
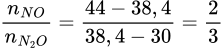 .
.► Quá trình cho-nhận e: Mg → Mg+2 + 2e (1) || 8N+5 + 30e → 2N+2 + 6N+1 (2).
Thăng bằng electron: 15 × (1) + 1 × (2) ⇒ 15Mg + 8N+5 → 15Mg+2 + 2N+2 + 6N+1.
● Điền hệ số: 15Mg + HNO3 → 15Mg(NO3)2 + 2NO + 3N2O + H2O.
Chú ý: chưa điền hệ số vào HNO3 vì 1 phần N+5 (NO3–) đóng vai trò môi trường.
Bảo toàn nguyên tố Nitơ ⇒ 38HNO3. Bảo toàn nguyên tố Hidro ⇒ 19H2O.
||⇒ 15Mg + 38HNO3 → 15Mg(NO3)2 + 2NO + 3N2O + 19H2O.
► Phân tử bị khử là N trong sản phẩm khử (cụ thể là NO và N2O),
phân tử bị oxi hóa là Mg ⇒ tỉ lệ là (2 + 3 × 2) : 15 = 8 : 15 ⇒ chọn A.