Cho từ từ dung dịch Ba(OH)2 vào dung dịch Al2(SO4)3 thấy số mol Ba(OH)2 bằng 0,9 hoặc 1,0 mol thì số mol kết tủa đều là 3a. Còn nếu số mol Ba(OH)2 bằng 0,7 mol thì số mol kết tủa là 4a. Số mol Al2(SO4)3 ban đầu là
-
-
-
-
Đáp án đúng: A
Giải: gt ⇒ tại 0,9 hay 1 mol thì Al(OH)3 tan hết, ↓ chỉ có BaSO4.
⇒ nBaSO4 = 3a mol ⇒ nAl2(SO4)3 = a mol ||– Tại 0,7 mol Ba(OH)2:
TH1: Al(OH)3 chưa max ⇒ nBaSO4 = nBa2+ = 0,7 mol;
nAl(OH)3 = nOH– ÷ 3 = 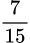 mol ⇒ 0,7 +
mol ⇒ 0,7 + 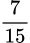 = 4a ⇒ a =
= 4a ⇒ a = 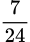 mol.
mol.
⇒ nOH : nAl3+ = 4,8 ⇒ Al(OH)3 tan hết ⇒ vô lí.
TH2: Al(OH)3 bị tan 1 phần ⇒ nBaSO4 = 3a mol.
⇒ nAl(OH)3 = a mol = 4 × 2a – 0,7 × 2 ⇒ a = 0,2 mol ⇒ chọn A.
Số bình luận về đáp án: 23
⇒ nBaSO4 = 3a mol ⇒ nAl2(SO4)3 = a mol ||– Tại 0,7 mol Ba(OH)2:
TH1: Al(OH)3 chưa max ⇒ nBaSO4 = nBa2+ = 0,7 mol;
nAl(OH)3 = nOH– ÷ 3 =
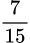 mol ⇒ 0,7 +
mol ⇒ 0,7 + 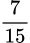 = 4a ⇒ a =
= 4a ⇒ a = 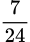 mol.
mol.⇒ nOH : nAl3+ = 4,8 ⇒ Al(OH)3 tan hết ⇒ vô lí.
TH2: Al(OH)3 bị tan 1 phần ⇒ nBaSO4 = 3a mol.
⇒ nAl(OH)3 = a mol = 4 × 2a – 0,7 × 2 ⇒ a = 0,2 mol ⇒ chọn A.