Đốt cháy hỗn hợp gồm Fe, S với oxi sau một thời gian thu được 23,68 gam hỗn hợp X chứa muối sunfua và các oxit sắt. Hòa tan hết X trong dung dịch HCl 14,6% (vừa đủ) đun nóng thu đươc dung dịch Y. Cho dung dịch AgNO3 dư vào dung dịch Y thu được 114,86 gam kết tủa. Mặt khác hòa tan hết X trong dung dịch H2SO4 đặc, nóng dư thu được 16,128 lít khí SO2 (sản phẩm khử duy nhất, đktc). Giả sử nước bay hơi không đáng kể. Nồng độ C% của FeCl3 có trong dung dịch Y?
-
-
-
-
Đáp án đúng: B
Coi hỗn hợp X gồm Fe x mol, S y mol, O : z mol → 56x + 32y + 16z = 23,68
TN1 :Ta có toàn bộ S, O trong X chuyển thành H2S: y mol và H2O : z mol
Bảo toàn nguyên tố H → nHCl = 2nH2S + 2nH2O → nAgCl = nHCl = 2y + 2z
Khi cho dung dịch Y tác dụng với AgNO3 dư thu được chất rắn chứa AgCl và Ag, dung dịch chứa Fe(NO3)3
Bảo toàn electron cho toàn bộ quá trình → 3nFe = 2nS + 2nO + nAg → 3x = 2y + 2z + nAg → nAg = nFe2+ = 3x-2y-2z
Vây 114,86 = 108 (3x-2y-2z) + 143,5 (2y + 2z)
TN2 : Bảo toàn electron cho toàn bộ quá trình → 3nFe + 6nS = 2nO + 2nSO2 → 3x + 6y -2z = 0,72.2
Ta có hệ 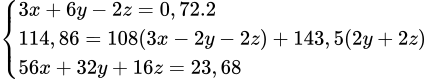 →
→ 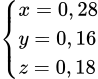
Vậy nFe2+ = nAgCl = 0,16 mol → nFe3+ = 0,28-0,16 = 0,12 mol
Ta có mddHCl = 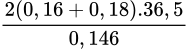 = 170 gam
= 170 gam
→ mY = mX + mHCl - mH2S = 23,68 + 170 - 0,16.34= 188,24
% FeCl3 = 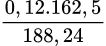 ×100% = 10,36%.
×100% = 10,36%.
Số bình luận về đáp án: 1
TN1 :Ta có toàn bộ S, O trong X chuyển thành H2S: y mol và H2O : z mol
Bảo toàn nguyên tố H → nHCl = 2nH2S + 2nH2O → nAgCl = nHCl = 2y + 2z
Khi cho dung dịch Y tác dụng với AgNO3 dư thu được chất rắn chứa AgCl và Ag, dung dịch chứa Fe(NO3)3
Bảo toàn electron cho toàn bộ quá trình → 3nFe = 2nS + 2nO + nAg → 3x = 2y + 2z + nAg → nAg = nFe2+ = 3x-2y-2z
Vây 114,86 = 108 (3x-2y-2z) + 143,5 (2y + 2z)
TN2 : Bảo toàn electron cho toàn bộ quá trình → 3nFe + 6nS = 2nO + 2nSO2 → 3x + 6y -2z = 0,72.2
Ta có hệ
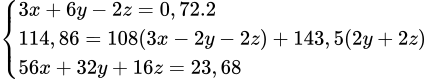 →
→ 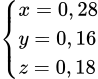
Vậy nFe2+ = nAgCl = 0,16 mol → nFe3+ = 0,28-0,16 = 0,12 mol
Ta có mddHCl =
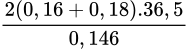 = 170 gam
= 170 gam→ mY = mX + mHCl - mH2S = 23,68 + 170 - 0,16.34= 188,24
% FeCl3 =
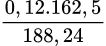 ×100% = 10,36%.
×100% = 10,36%.