Dung dịch HF có pH=2 hằng số axit của HF : Ka= 6,8.10-4.Nồng độ mol/l của dung dịch HF ban đầu bằng:
-
-
-
-
Đáp án đúng: A
HF ⇄ H+ + F- Ka = 6,8. 10-4
Gọi nồng độ của HF ban đầu là x
Dung dịch có pH = 2 → [H+] =[F-]= 0,01M
Nồng độ của HF ở trạng thái cân bằng là → [HF] = x- 0,01
Có Ka =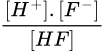 =
= 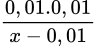 = 6,8. 10-4 → x = 0,157M
= 6,8. 10-4 → x = 0,157M
Đáp án A.
Số bình luận về đáp án: 0
Gọi nồng độ của HF ban đầu là x
Dung dịch có pH = 2 → [H+] =[F-]= 0,01M
Nồng độ của HF ở trạng thái cân bằng là → [HF] = x- 0,01
Có Ka =
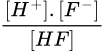 =
= 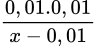 = 6,8. 10-4 → x = 0,157M
= 6,8. 10-4 → x = 0,157MĐáp án A.