Hòa tan hết 28,16 gam hỗn hợp rắn X gồm Mg, Fe3O4 và FeCO3 vào dung dịch chứa H2SO4 và NaNO3, thu được 4,48 lít (đktc) hỗn hợp khí Y (gồm CO2, NO, N2, H2) có khối lượng 5,14 gam và dung dịch Z chỉ chứa các muối trung hòa. Dung dịch Z phản ứng tối đa với 1,285 mol NaOH, thu được 43,34 gam kết tủa và 0,56 lít khí (đktc). Nếu cho Z tác dụng với dung dịch BaCl2 dư thì thu được 166,595 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng của Mg trong X là
-
-
-
-
Đáp án đúng: B
HD: Sơ đồ quá trình phản ứng và xử lí:
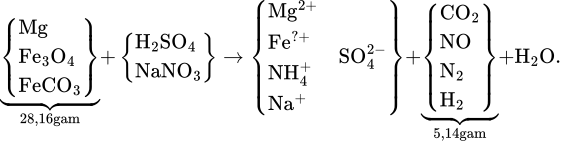
166,595 gam kết tủa là 0,715 mol BaSO4 → có nH2SO4 = ∑nSO42– = 0,715 mol.
0,56 lít khí là 0,025 mol NH4+. Dùng YTHH 02: Natri đi về đâu? 0,715 mol Na2SO4
⇒ nNa+ trong Z = 0,715 × 2 – 1,285 = 0,145 mol → có 0,145 mol NaNO3.
trong Z: 0,145 mol Na+; 0,025 mol NH4+ ⇒ ∑nSO42– kết hợp cation Mg2+, Fe?+ = 1,26 mol.
⇒ 43,34 gam kết tủa gồm: Mg, Fe và 1,26 mol OH ⇒ ∑mMg, Fe = 21,92 gam.
⇝ BTKL cả sơ đồ có mH2O = 11,07 gam ⇒ nH2O = 0,615 mol.
⇒ bảo toàn nguyên tố H có nH2 trong Y = 0,05 mol.
Y gồm CO2, N2, NO và 0,05 mol; tổng 0,2 mol; nặng 5,14 gam.
bảo toàn N có thêm giả thiết nNO + 2nN2 = 0,12 mol ⇒ giải hệ số mol 3 khí còn lại:
nNO = 0,1 mol; nN2 = 0,01 mol; nCO2 = 0,04 mol ⇝ có 0,04 mol FeCO3.
từ đó có: nFe3O4 = (28,16 – 21,92 – 0,04 × 60) ÷ 16 ÷ 4 = 0,06 mol.
Từ đó có mMg = 9,6 gam ⇒ %mMg trong X = 9,6 ÷ 28,16 × 100% ≈ 34,09% ⇝ Chọn đáp án B. ♦
Số bình luận về đáp án: 2

166,595 gam kết tủa là 0,715 mol BaSO4 → có nH2SO4 = ∑nSO42– = 0,715 mol.
0,56 lít khí là 0,025 mol NH4+. Dùng YTHH 02: Natri đi về đâu? 0,715 mol Na2SO4
⇒ nNa+ trong Z = 0,715 × 2 – 1,285 = 0,145 mol → có 0,145 mol NaNO3.
trong Z: 0,145 mol Na+; 0,025 mol NH4+ ⇒ ∑nSO42– kết hợp cation Mg2+, Fe?+ = 1,26 mol.
⇒ 43,34 gam kết tủa gồm: Mg, Fe và 1,26 mol OH ⇒ ∑mMg, Fe = 21,92 gam.
⇝ BTKL cả sơ đồ có mH2O = 11,07 gam ⇒ nH2O = 0,615 mol.
⇒ bảo toàn nguyên tố H có nH2 trong Y = 0,05 mol.
Y gồm CO2, N2, NO và 0,05 mol; tổng 0,2 mol; nặng 5,14 gam.
bảo toàn N có thêm giả thiết nNO + 2nN2 = 0,12 mol ⇒ giải hệ số mol 3 khí còn lại:
nNO = 0,1 mol; nN2 = 0,01 mol; nCO2 = 0,04 mol ⇝ có 0,04 mol FeCO3.
từ đó có: nFe3O4 = (28,16 – 21,92 – 0,04 × 60) ÷ 16 ÷ 4 = 0,06 mol.
Từ đó có mMg = 9,6 gam ⇒ %mMg trong X = 9,6 ÷ 28,16 × 100% ≈ 34,09% ⇝ Chọn đáp án B. ♦