Hòa tan hoàn toàn 20,48 gam hỗn hợp gồm K, K2O, Al và Al2O3 vào H2O (dư), thu được dung
dịch X và 0,18 mol khí H2. Cho t?
Hòa tan hoàn toàn 20,48 gam hỗn hợp gồm K, K2O, Al và Al2O3 vào H2O (dư), thu được dung dịch X và 0,18 mol khí H2. Cho từ từ dung dịch HCl 1M vào X, lượng kết tủa Al(OH)3 (a mol) phụ thuộc vào thể tích dung dịch HCl (V ml) được biểu diễn bằng đồ thị sau:
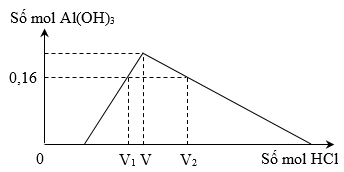
Biết tỉ lệ V2 : V1 = 5 : 3. Giá trị của V là

Biết tỉ lệ V2 : V1 = 5 : 3. Giá trị của V là
A. 280.
B. 200.
C. 340.
D. 260.
Đáp án A
Giải: Quy đổi hỗn hợp X thành Al2O3 và K2O với mHỗn hợp = 20,48 + 0,18×16 = 23,36 gam.Sơ đồ ta có: \(\left\{ \begin{array}{l}A{l_2}{O_3}:a\\{K_2}O:b\end{array} \right. + {H_2}O \to \left\{ \begin{array}{l}KO{H_{du}}:2b - 2a\\KAl{O_2}:2a\end{array} \right.\). ⇒ 102a + 94b = 23,36 (1)
⇒ nHCl ứng với V1 = (2b – 2a) + 0,16.
⇒ nHCl ứng với V2 = (2b – 2a) + 2a + (2a–0,16)×3 = 6a + 2b – 0,48
⇒ \(\dfrac{V_1}{V_2} = \dfrac{2b-2a+0,16}{6a+2b-0,48} = \dfrac{3}{5} \) \(\Leftrightarrow\) 28a – 4b = 2,24 (2)
+ Giải hệ (1) và (2) ⇒ nAl2O3 = 0,1 và nK2O = 0,14.
⇒ Số mol HCl cần để tạo kết tủa cực đại = 2b – 2a + 2a = 2b = 0,28 mol.
⇒ VHCl = \(\dfrac{0,28}{1}\) = 0,28 lít = 280 ml ⇒ Chọn A







