Hoà tan hoàn toàn 2,56 gam Cu vào 25,20 gam dung dịch HNO3 60% thu được dung dịch X (không có ion NH4+). Thêm 210 ml dung dịch NaOH 1M vào X, sau khi các phản ứng kết thúc đem cô cạn hỗn hợp thu được chất rắn Y. Nung Y đến khối lượng không đổi được 17,40 gam chất rắn Z. Nồng độ % của Cu(NO3)2 trong dung dịch X có giá trị gần nhất với
-
-
-
-
Đáp án đúng: C
Nhận thấy nếu dung dịch NaOH vừa đủ thì chất rắn thu được chỉ chứa NaNO2: 0,21 mol và CuO : 0,04 → mZ = 0,21.69+ 0,04. 80 = 17,69 > 17,4 gam → Chất rắn Z chứa NaOH dư, CuO, NaNO2
0,04 mol Cu 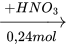 Dd X
Dd X 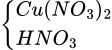
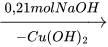 chất rắn Y
chất rắn Y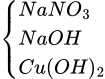
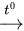 17,4 gam
17,4 gam 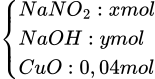
Bảo toàn nguyên tố Na → x+ y = 0, 21
Theo đề bài 69x+ 40y + 0,04. 80 = 17,4 → x= 0,2 và y = 0,01
Gọi sản phẩm khử chứa N và O
Nhận thấy toàn bộ NO3- trong dung dịch X chuyển hết về NO3- trong NaNO3
→ nNO3- ( trong X) = nNaNO3= 0,2mol
Bảo toàn nguyên tố N → nN(khí) = 0,24- 0,2 = 0,04 mol
Bảo toàn electron cho toàn bộ quá trình → 2nO(khí)= 5nN- 2nCu → nO ( khí)= (0,04.5 - 2. 0,04) : 2=0,06 mol
mdd= 2,56 + 25,2- 0,06.16 - 0,04.14= 26,24 gam
→ %Cu(NO3)2 = 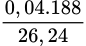 ×100%= 28,66%. Đáp án C.
×100%= 28,66%. Đáp án C.
Số bình luận về đáp án: 48
0,04 mol Cu
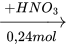 Dd X
Dd X 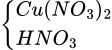
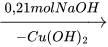 chất rắn Y
chất rắn Y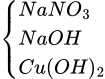
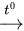 17,4 gam
17,4 gam 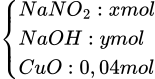
Bảo toàn nguyên tố Na → x+ y = 0, 21
Theo đề bài 69x+ 40y + 0,04. 80 = 17,4 → x= 0,2 và y = 0,01
Gọi sản phẩm khử chứa N và O
Nhận thấy toàn bộ NO3- trong dung dịch X chuyển hết về NO3- trong NaNO3
→ nNO3- ( trong X) = nNaNO3= 0,2mol
Bảo toàn nguyên tố N → nN(khí) = 0,24- 0,2 = 0,04 mol
Bảo toàn electron cho toàn bộ quá trình → 2nO(khí)= 5nN- 2nCu → nO ( khí)= (0,04.5 - 2. 0,04) : 2=0,06 mol
mdd= 2,56 + 25,2- 0,06.16 - 0,04.14= 26,24 gam
→ %Cu(NO3)2 =
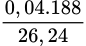 ×100%= 28,66%. Đáp án C.
×100%= 28,66%. Đáp án C.