pH của dung dịch hỗn hợp gồm CH3COOH 0,1M (Ka=1,75.10-5 ) và CH3COONa 0,1M là
-
-
-
-
Đáp án đúng: B
CH3COONa → CH3COO- + Na+
0,1...................0,1........0,1
CH3COOH ⇄ CH3COO- + H+ Ka = 1,75. 10-5
Tại thời điểm cân bằng gọi nồng độ của H+ là xM, [CH3COOH] = 0,1-x, CH3COO- = 0,1 + x (M)
Có Ka =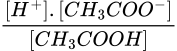 =
= 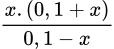 = 1,75. 10-5 → x = 1,75.10-5
= 1,75. 10-5 → x = 1,75.10-5
→ pH = -log (1,75.10-5) = 4,756. Đáp án B.
Số bình luận về đáp án: 0
0,1...................0,1........0,1
CH3COOH ⇄ CH3COO- + H+ Ka = 1,75. 10-5
Tại thời điểm cân bằng gọi nồng độ của H+ là xM, [CH3COOH] = 0,1-x, CH3COO- = 0,1 + x (M)
Có Ka =
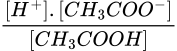 =
= 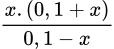 = 1,75. 10-5 → x = 1,75.10-5
= 1,75. 10-5 → x = 1,75.10-5→ pH = -log (1,75.10-5) = 4,756. Đáp án B.