Phản ứng giữa Na2S2O3 và H2SO4 thu được muối sulfate, sulfur, sulful dioxide và nước, thường được dùng trong nghiên cứu các yếu tố ảnh hưởng đến tốc độ phản ứng. Tiến hành thí nghiệm với 100 ml dung dịch hỗn hợp Na2S2O3 0,5M và H2SO4 (dư), sau 40 giây, thể tích SO2 thu được ở điều kiện chuẩn là 0,9916 L. Giả sử khí tạo ra đều thoát ra khỏi dung dịch, tính tốc độ trung bình của phản ứng theo Na2S2O3.
-
-
-
-
Đáp án đúng:
HD: Ta có nSO2 = 0,9916 ÷ 24,79 = 0,04 mol.
Phương trình phản ứng: Na2S2O3 + H2SO4 → Na2SO4 + SO2 + S + H2O.
⇒ từ tỉ lệ phản ứng ta có nNa2S2O3 phản ứng = 0,04 mol ⇒ [Na2S2O3] = 0,04 ÷ 0,1 = 0,4 M.
Tốc độ trung bình của phản ứng tính theo Na2S2O3 là:
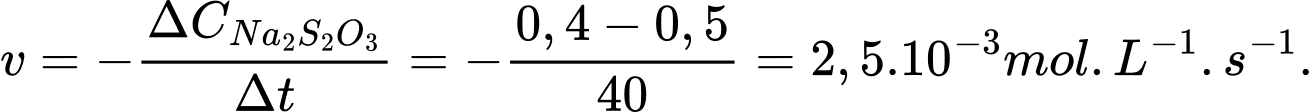 Số bình luận về đáp án: 24
Số bình luận về đáp án: 24
Phương trình phản ứng: Na2S2O3 + H2SO4 → Na2SO4 + SO2 + S + H2O.
⇒ từ tỉ lệ phản ứng ta có nNa2S2O3 phản ứng = 0,04 mol ⇒ [Na2S2O3] = 0,04 ÷ 0,1 = 0,4 M.
Tốc độ trung bình của phản ứng tính theo Na2S2O3 là: