(2) Nguyên tử H trong H2S và H2O đạt được cấu hình bền vững của khí hiếm
(3) Để hình hành liên kết trong phân tử H2S và H2O các orbital nguyên tử xen phủ trục với nhau tạo ra liên kết
(4) Nhiệt độ sôi của H2O cao hơn H2S là do H2O có
(b) tương tác van der Waals
(c) helium
(d) cộng hóa trị
(e) ion
(g) neon
(h) sigma (
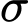 )
)