Tiến hành điện phân dung dịch chứa m gam hỗn hợp CuSO4 và NaCl (hiệu suất 100%, điện cực trơ, màng ngăn xốp), đến khi nước bắt đầu bị điện phân ở cả hai điện cực thì ngừng điện phân, thu được dung dịch X và 6,72 lít khí (đktc) ở anot. Dung dịch X hòa tan tối đa 20,4 gam Al2O3. Giá trị của m là
-
-
-
-
Đáp án đúng: C
Giải: ► GIẢ SỬ Al2O3 bị hòa tan bởi H+: Al2O3 + 6H+ → 2Al3+ + 3H2O.
⇒ nH+ = 1,2 mol || Lại có: 2H2O → 4H+ + O2↑ + 4e ⇒ nO2 = 0,3 mol = ∑nkhí/anot ⇒ vô lí!.
⇒ Al2O3 bị hòa tan bởi OH– || Al2O3 + 2OH– → 2AlO2– + H2O ⇒ nOH– = 0,4 mol.
► Khí ở anot chỉ có Cl2 ⇒ nCl2 = 0,3 mol. Xét quá trình điện phân ở 2 cực:
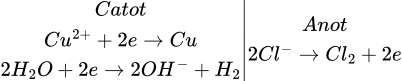
Bảo toàn electron: 2nCu2+ + nOh– = 2nCl2 ⇒ nCu2+ = 0,1 mol.
||⇒ m = 0,1 × 160 + 0,6 × 58,5 = 51,1(g) ⇒ chọn C.
Số bình luận về đáp án: 18
⇒ nH+ = 1,2 mol || Lại có: 2H2O → 4H+ + O2↑ + 4e ⇒ nO2 = 0,3 mol = ∑nkhí/anot ⇒ vô lí!.
⇒ Al2O3 bị hòa tan bởi OH– || Al2O3 + 2OH– → 2AlO2– + H2O ⇒ nOH– = 0,4 mol.
► Khí ở anot chỉ có Cl2 ⇒ nCl2 = 0,3 mol. Xét quá trình điện phân ở 2 cực:
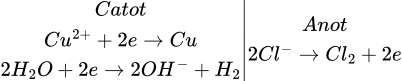
Bảo toàn electron: 2nCu2+ + nOh– = 2nCl2 ⇒ nCu2+ = 0,1 mol.
||⇒ m = 0,1 × 160 + 0,6 × 58,5 = 51,1(g) ⇒ chọn C.