Tiến hành phản ứng nhiệt nhôm với Fe2O3 trong điều kiện không có không khí. Chia hỗn hợp thu được sau phản ứng (đã trộn đều) thành 2 phần không bằng nhau. Phần 2 có khối lượng nhiêu hơn phần 1 là 134 gam. Cho phần 1 tác dụng với lượng dư dung dịch NaOH thấy có 16,8 lít khí H2 bay ra. Hòa tan phần 2 bằng lượng dư dung dịch H2SO4 loãng thấy có 84 lít khí H2 bay ra. Các phản ứng đều xảy ra với hiệu suất 100%. Các khí đo ở đktc. Khối lượng Fe tạo thành trong phản ứng nhiệt nhôm gần nhất là
-
-
-
-
Đáp án đúng: B
Fe2O3 + 2Al → Al2O3 + 2Fe
Nhận thấy P1 tác dụng với NaOH sinh khí → sau phản ứng chứa Al, Al2O3 và Fe
Có nAl = 2nH2 :3 = 0,5 mol
Phần 1 gọi số mol của Al2O3 , Fe lần lượt là x, 2x
→ phần 2 số mol của Al, Al2O3 , Fe lần lượt là 0,5k, kx, 2kx → 0,5k. 3 + 2.2kx = 2nH2 =7,5 → x = 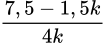 =
=
Có 27.0,5k +102kx+ 56.2xk - 27. 0,5 - 102x - 56.2x = 134 → 13,5k + 214.k. 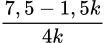 - 214.
- 214. 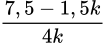 = 147,5
= 147,5
→ -267k2 + 1336k-1605= 0 → k = 2 hoặc k = 3
Với k = 2 → x = 0,5625 → m Fe = 2. (0,5625 + 0,5625.2). 56 = 189 gam
Với k = 3 → x = 0,25→ m Fe = 2.(0,25+0,25.3). 56 = 112 gam . Đáp án B.
Số bình luận về đáp án: 1
Nhận thấy P1 tác dụng với NaOH sinh khí → sau phản ứng chứa Al, Al2O3 và Fe
Có nAl = 2nH2 :3 = 0,5 mol
Phần 1 gọi số mol của Al2O3 , Fe lần lượt là x, 2x
→ phần 2 số mol của Al, Al2O3 , Fe lần lượt là 0,5k, kx, 2kx → 0,5k. 3 + 2.2kx = 2nH2 =7,5 → x =
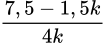 =
= Có 27.0,5k +102kx+ 56.2xk - 27. 0,5 - 102x - 56.2x = 134 → 13,5k + 214.k.
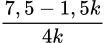 - 214.
- 214. 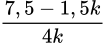 = 147,5
= 147,5→ -267k2 + 1336k-1605= 0 → k = 2 hoặc k = 3
Với k = 2 → x = 0,5625 → m Fe = 2. (0,5625 + 0,5625.2). 56 = 189 gam
Với k = 3 → x = 0,25→ m Fe = 2.(0,25+0,25.3). 56 = 112 gam . Đáp án B.