Tốc độ phản ứng giữa KMnO4 và H2C2O4 có thể được xác định qua sự thay đổi màu của dung dịch do biến thiên nồng độ của ion MnO4- . Khi tiến hành phản ứng ở nhiệt độ không đổi 25oC, người ta thu được các số liệu sau: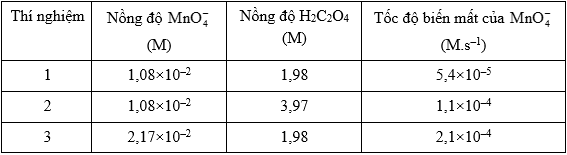
Bảng 6.26. Nồng độ các chất tham gia phản ứng và tốc độ trung bình của phản ứng ở các lần thí nghiệm khác nhau Xác định bậc phản ứng riêng phần của MnO4- và H2C2O4.
-
-
-
-
Đáp án đúng:
Biểu thức định luật tác dụng khối lượng: V = k.[H2C2O4]m.[ MnO4-]n
Ta có:
v1 = k.[1,98]m.[ 1,08.10-2]n = 5,4.10-5 (1)
v2 = k.[3,97]m.[ 1,08.10-2]n = 1,1.10-4 (2)
v3 = k.[1,98]m.[ 2,17.10-2]n = 2,1.10-4 (3)
Từ (1), (2) và (3) ta tìm được m =1; n = 2
Số bình luận về đáp án: 0

Bảng 6.26. Nồng độ các chất tham gia phản ứng và tốc độ trung bình của phản ứng ở các lần thí nghiệm khác nhau
Xác định bậc phản ứng riêng phần của MnO4- và H2C2O4.
Ta có:
v1 = k.[1,98]m.[ 1,08.10-2]n = 5,4.10-5 (1)
v2 = k.[3,97]m.[ 1,08.10-2]n = 1,1.10-4 (2)
v3 = k.[1,98]m.[ 2,17.10-2]n = 2,1.10-4 (3)
Từ (1), (2) và (3) ta tìm được m =1; n = 2