Trong dung dịch axit axetic tồn tại cân bằng Thực hiện các biện pháp sau: (1) nhỏ thêm vài giọt dung dịch HCl; (2) nhỏ t?
Trong dung dịch axit axetic tồn tại cân bằng 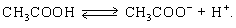
Thực hiện các biện pháp sau: (1) nhỏ thêm vài giọt dung dịch HCl; (2) nhỏ thêm vài giọt dung dịch NaOH; (3) nhỏ thêm vài giọt dung dịch CH3COONa; (4) tăng nồng độ dung dịch; (5) thêm nước cất vào pha loãng dung dịch. Những biện pháp nào làm độ điện li α của axit tăng?
Thực hiện các biện pháp sau: (1) nhỏ thêm vài giọt dung dịch HCl; (2) nhỏ thêm vài giọt dung dịch NaOH; (3) nhỏ thêm vài giọt dung dịch CH3COONa; (4) tăng nồng độ dung dịch; (5) thêm nước cất vào pha loãng dung dịch. Những biện pháp nào làm độ điện li α của axit tăng?
A. (1); (3); (4).
B. (2); (5).
C. (2); (4); (5).
D. (1); (4).
Đáp án B
HD: Dạng này nhầm và rất dễ nhầm → sai lầm với dạng cân bằng hóa học và tốc độ hóa học.đó là việc tăng nồng độ dung dịch (số (4)).
Độ điện li α = [số phân tử phân li] ÷ [số phân tử đem hòa tan] (*).
Việc tăng nồng độ → cả mẫu số và tử số cùng tăng → không giải quyết được vấn đề gì,
và thực tế c/m rằng α sẽ giảm (do nhiều nguyên nhân trong đó có ảnh hưởng của không gian,
H2O xung quanh). → (4) sai, chọn ngay đáp án C.
Các phương án còn lại, (1) bổ sung H+ sẽ làm tăng khả năng kết hợp tạo lại CH3COOH
nên tử số (*) giảm → α giảm; (3) thêm CH3COONa phân li hoàn toàn ra CH3COO- và Na+
dẫn đến kết quả tương tự (1); (2) khi cho OH- thì sẽ lấy H+ → H2O nên số phân tử axit bị phân li tăng
→ α tăng. (5) được giải thích là sẽ ngăn cách các ion tái tạo lại phân tử axit mà lại không ảnh hướng đến các phân tử phân li bình thường.


